Yazar: Sude Sak
Yağ dokusu, enerji metabolizmasında önemli bir rol oynayan bir bağ dokusu türüdür ve adiposit hücrelerini içerir. Küçük kan damarları ile yakından ilişkili olan adipositler, genellikle fibröz septa ile çevrili lobüller içinde tek tek veya gruplar halinde bulunur. Adipoz doku farklı hücre tipleri içerir. Dokunun sadece üçte biri adipositlerden oluşur. Geri kalanını fibroblastlar, makrofajlar, stromal hücreler, monositler ve preadipositler oluşturur.
Yağ dokusu, bir kalori rezervuarı olarak hareket ederek sistemik enerji homeostazının kritik bir düzenleyicisidir. Besin fazlalığı koşullarında, yağ dokusu fazla besinleri nötr lipidler şeklinde depolarken, besin eksikliği koşullarında lipoliz yoluyla diğer dokulara besin sağlar.
Vücudun enerji ihtiyacını karşılamak amacıyla lipitlerin sentezlenmesi ve depolanmasında görev alan, hücre sayısı ve büyüklüğü açısından hacmi sürekli değişen dinamik bir dokudur. Fazla enerji, trigliserit formundaki lipit damlacıklarında depolanır.
İnsanlarda metabolik enerji depolamanın en yoğun şekli olan trigliseritler, karbonhidrat ve proteinlerden iki kat daha fazla enerji depolar.
Eş zamanlı olarak, yağ dokusundaki çeşitli stromal vasküler hücreler sayısal ve/veya işlevsel değişikliklere uğrayarak yağ dokusunun bir enerji deposu ve endokrin organ olarak işlevini sürdürmesine katkıda bulunur.
Üç tür yağ dokusu vardır
Beyaz yağ dokusu (White adipose tissue-WAT) insan vücudundaki baskın yağ türüdür. WAT’ın enerji depolama, ısı kaybını önleme, hayati organları koruma ve hormon salgılama gibi çeşitli biyolojik işlevleri vardır. Bazı hormonlar arasında leptin, adiponektin ve resistin bulunur.
Üçüncü ve en yeni adiposit türü olan bej adiposit dokusu, WAT’ın esmerleşmesi olarak bilinen bir süreç olan termojenik stimülasyona yanıt olarak WAT’ta ortaya çıkabilir. Son araştırmalar, WAT’ın kahverengileşmesinin daha fazla ilgiyi hak ettiğini ve WAT’ın kahverengileşmesini hedefleyen tedavilerin obeziteyi azaltmaya yardımcı olabileceğini göstermektedir. Bej adipositler WAT içinde bulunur ve soğuğa maruz kalma sırasında ısı üretmek için enerji harcar (soğuğa bağlı termojenez olarak adlandırılır). Aktive edilmiş bej yağ dokusunun kilo kaybını uyarabildiği ve obeziteye karşı direnci artırabildiği iyi bilinmektedir, bu da onu çekici bir terapötik hedef doku haline getirmektedir. Yaşlanma obezite için birincil risk faktörüdür ve bej yağ dokusu kaybıyla ilişkilidir, bu da enerji harcama kapasitelerinin kaybının artan yaşla birlikte obeziteye eğilimli bir fenotipe katkıda bulunabileceğini düşündürmektedir.
Hemen hemen her memelide kahverengi yağ dokusu (Brown adipose tissue-BAT) bulunur. Yeni doğanlarda ve kış uykusuna yatan memelilerde kahverengi yağ dokusu özellikle bol miktarda bulunur. Yetişkinlerde de bulunur ve metabolik olarak aktiftir, ancak yaygınlığı yaşla birlikte azalır. Bu bezin birincil işlevi termoregülasyondur. BAT hücrelerinin mitokondrilerinin, çok miktarda sitokrom bulunması nedeniyle kahverengi renkte olduğu gözlemlenmiştir. Kış uykusu bezi olarak da adlandırılır çünkü bu yağ depoları hayvanın kış uykusundan uyanması sırasında işlev görür.
Enerji Metabolizması
Lipidlerin metabolizması ve mobilizasyonu adipoz dokunun kontrolü altındadır. Lipogenez, karbonhidratların yağ asitlerine dönüştürüldüğü, trigliseritlerin (TG) biyosentezini ve adipositler içinde lipit damlacıklarının genişlemesini teşvik eden süreçtir. Tersine, lipoliz TG’yi oksitlenebilen veya serbest bırakılabilen serbest yağ asitlerine (FFA) ve gliserole parçalar.
Dolaşımdaki FFA’ların karaciğer, kaslar ve diğer dokular tarafından alınması, lipid mobilizasyonu için birincil yolu oluşturur. Hem lipogenez hem de lipoliz yolları beslenme faktörlerine ve insülin, norepinefrin ve glukagon gibi hormonlara karşı oldukça hassastır. Sonuç olarak, bu süreçlerin karmaşık bir şekilde düzenlenmesi, sistemik enerji homeostazının ve insülin duyarlılığının korunması için gereklidir.
Lipogenez ve Lipoliz
Lipogenez, asetil koenzim A’dan trigliseritlerin ve yağ asitlerinin sentezini tanımlamak için kullanılan terimdir. Buna karşılık, lipoliz trigliseritlerin parçalanmasını içerir ve yağ asitlerinin oluşumuna yol açar. Bu iki süreç arasındaki temel ayrım, temel yapılarında yatmaktadır. Özellikle lipoliz, yağların ve çeşitli lipit moleküllerinin hidrolizine odaklanır ve yağ asitlerinin üretimiyle sonuçlanır. Tersine, lipogenez, asetil koenzim A ve diğer öncüler gibi substratlardan yağ asitleri ve trigliseritlerin oluşturulmasını gerektirir.
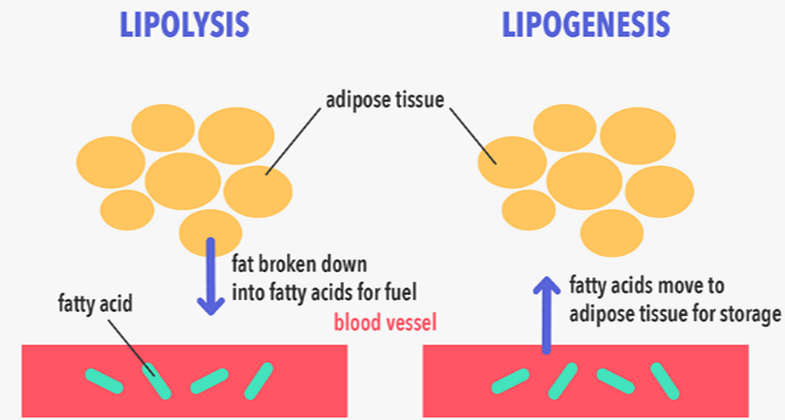
Adipoz doku, sırasıyla lipogenez ve lipoliz adı verilen süreçlerle yağ asitleri olarak salınan TG’ler barındıran önemli bir enerji depolama rezervuarı olarak hizmet eder.
Sistemik gıda alımı lipojenik yolun aktivasyonunu tetikleyerek yağ dokusunda TG depolanmasını teşvik eder. Buna karşılık, açlık lipolitik yolu başlatarak TG’lerin parçalanmasını ve ardından yağ asitlerinin adipoz depolarından salınmasını sağlar. Bu karmaşık denge, asetil-koenzim A’dan (asetil-CoA) taze yağ asitleri oluşturma süreci olan lipogenezi ve TG sentezini içerir.
Glikoz metabolizması, yağ asidi sentezi için çok önemli bir bileşen olan asetil-CoA üretir. Bu süreç aynı zamanda lipogenezde hızı kontrol eden enzim olan asetil-CoA karboksilazın ekspresyonunu artırır ve pankreatik insülin salınımını tetikleyerek lipogenezi daha da ilerletir. Özünde, yağ dokusu bir enerji rezervuarı olarak işlev görür, yağ asidi akışlarını etkili bir şekilde azaltır ve lipotoksisite ve insülin direncini önler. Bu doku aynı zamanda plazma TG’lerinin temizlenmesini yöneterek diğer vücut dokularında birikmesini önler.
Sonuç olarak, yağ dokusunun lipit depolama kapasitesi, sistemik insülin direncinde ve lipitlerin karaciğer ve kas gibi organlara sızmasında önemli bir rol oynar. Aksine, lipoliz, depolanan TG’lerin adipositler içinde katabolik olarak parçalanmasını ve serbest yağ asitleri ile gliserolün açığa çıkmasını gerektirir.
Açlık lipolizi tetikleyerek hepatik glukoneogenez için gliserol ve oksidasyon için serbest yağ asitleri verir ve diğer organların enerji gereksinimlerini karşılar. Yağ asitleri bol ve karbonhidratlar az olduğunda, karaciğer keton cisimleri oluşturmak için yağ asitlerini daha fazla metabolize edebilir, bu süreç ketogenez olarak adlandırılır ve beyin için bir enerji kaynağı olarak hizmet eder. Lipogenez ve lipoliz arasındaki bu dinamik etkileşim, sistemik enerji dengesini ve insülin duyarlılığını korumak için çok önemlidir. Genel olarak, yağ dokusunun çok yönlü işlevleri, vücudun enerji homeostazında bir enerji rezervuarı ve düzenleyici olarak öneminin altını çizmektedir.
Yağ dokusu endokrin bir organ gibi hareket eder.
Beyaz yağ dokusu, temel adipokinlerin salgılanmasını sağlayarak lipid depolanması veya salınımı ve enerji dengesinde ikili bir rol oynayan çok önemli bir endokrin organ olarak ortaya çıkmaktadır. Bunlar arasında adipositler, glikoz ve lipid metabolizması homeostazı için çok önemli olan hassas bir dengeyi düzenleyen leptin, resistin ve adiponektin gibi polipeptitler salgılar. Adipositlerden yayılan bu adipositokinlerin karmaşık etkileşimi, optimal enerji seviyelerinin sürdürülmesine temelden katkıda bulunur.
Önemli bir oyuncu olan leptin, aşırı enerji alımı, insülin seviyeleri ve glikoz seviyeleri gibi faktörlere yanıt vererek değişen üretim oranlarına neden olur. Tersine, açlık, soğuğa maruz kalma, β-adrenerjik agonistler ve testosteron leptin salgılanmasının azalmasına yol açar. Yağ dokusu içinde sentezlenen kolajen benzeri bir plazma proteini olan adiponektin önemli bir rol oynar. Deri altı beyaz yağ dokusunda konsantrasyonu daha yüksekken, visseral beyaz yağ dokusu ve hipertrofik adipositler dolaşımdaki adiponektin seviyeleri ile ters orantılıdır. Kilo kaybı ve açlık dönemleri plazma adiponektin seviyelerinde bir artışı tetikler ve bu da kaslarda glikoz kullanımını aktive eder. Bu kaskad, karaciğer ve kaslarda yağ asidi oksidasyonunu artırır ve ardından inhibe edilmiş glukoneogenez nedeniyle glikoz üretimini engeller.
Uyarlanabilir termojenezin düzenlenmesi
Termogenin (uncoupling protein 1 veya UCP1), soğuk kaynaklı termojeneze özgü bir moleküldür ve kahverengi yağ dokusunda seçici olarak ifade edildiği için çok önemli bir rol üstlenir. Oksidatif fosforilasyonu ATP sentezinden uzaklaştırarak ve enerjiyi ATP üretimi yerine ısı üretimine yönlendirerek kayda değer bir metabolik değişim düzenler.
Soğuğa maruz kalma ve artan besin alımı, merkezi sinir sisteminden kaynaklanan norepinefrin ve UCP1’in yüksek ekspresyon seviyelerinin eşlik ettiği kahverengi yağ dokusu aktivitesinde bir artışı tetikler. Özellikle, β-adrenerjik antagonistler, tiroid hormonları, insülin ve cAMP analogları dahil olmak üzere bir dizi ajan da UCP1 ekspresyonunun artmasına katkıda bulunur.
Soğuğa ve besin mevcudiyetine yanıt olarak, sempatik sinir aktivitesi yağ dokusu içinde yoğunlaşır. Noradrenalin, β-adrenerjik reseptörlere ustalıkla bağlanır ve böylece trigliseritlerin hidroliziyle sonuçlanan bir dizi moleküler sinyali tetikler. Yağ asitlerinin serbest kalması ikili bir rol oynar, sadece UCP1’e enerji vermekle kalmaz, aynı zamanda soğuk kaynaklı termojenik yollarda termojenezi besler ve glikoz bozunma için özel karbon kaynağı olarak hizmet eder.
Özellikle, aktivasyon bej hücrelere kadar uzanarak termojenik yanıtı daha da artırır. Sonuç olarak, bu düzenlenmiş mekanizma tüm vücut enerji harcamasında bir artışa neden olurken aynı zamanda vücut yağ kütlesini azaltır. Özünde, bu karmaşık süreçlerin karşılıklı etkileşimi, enerji harcamasını artıran ve vücut yağ kütlesini azaltan metabolik bir senfoni düzenler.
Bu makale öğrencimiz Sude Sak’ın sunumundan hazırlanmıştır.
Referanslar
Bódis, K, Roden, M (2018). Energy metabolism of white adipose tissue and insulin resistance in humans. Eur J Clin Invest., 48:e13017. DOI: 10.1111/eci.13017
Choe SS, Huh JY, Hwang IJ, Kim JI, Kim JB (2016). Adipose Tissue Remodeling: Its Role in Energy Metabolism and Metabolic Disorders. Front Endocrinol (Lausanne), 7:30. DOI: 10.3389/fendo.2016.00030.
Mermer M, Tek NA (2017). Adipoz doku ve enerji metabolizması üzerine etkileri. Sdü Sağlık Bilimleri Enstitüsü Dergisi, 8(3): 40-46. DOI: 10.22312/sdusbed.292229
Wang Z, Wang QA, Liu Y, Jiang L (2021). Energy metabolism in brown adipose tissue. FEBS Journal, 288(12): 3647-3662. DOI: 10.1111/febs.16015.
Zhu Q, Glazier BJ, Hinkel BC, Cao J, Liu L, Liang C, Shi H (2019). Neuroendocrine Regulation of Energy Metabolism Involving Different Types of Adipose Tissues. Int J Mol Sci., 20(11): 2707. DOI: 10.3390/ijms20112707.
Yayın Tarihi: 10 Ağustos 2023Son Düzenleme: 10 Ağustos 2023